
Getty La imagen ilustrativa muestra a una mujer recibiendo y desempaquetando un paquete postal con pruebas rápidas de antígeno FlowFlex SARS-CoV-2BELGA PHOTO PHILIPPE FRANCOIS (Photo by PHILIPPE FRANCOIS/BELGA MAG/AFP via Getty Images)
Las pruebas caseras para la detección del virus del COVID-19 sin duda alguna, fue una gran herramienta para quienes, desde la comodidad de su hogar, y con la sospecha de ser portadores del virus, podían realizarse sin la necesidad de la ayuda de un profesional, ni esperando el resultado de un laboratorio, una prueba COVID y de dar positivos, tomar las precauciones pertinentes para no contagiar a los demás.
En los Estados Unidos, estás pruebas, se pueden conseguir en farmacias por un precio asequible de $10 a $15 dólares, y en algunos casos, son entregadas a un núcleo familiar de manera gratuita.
Ante su gran aprobación en la población, ¿qué podría salir mal con estas pruebas? Pues, en la última semana se conoció un reporte por parte de la Administración de Alimentos y Medicamentos (FDA por sus siglas en inglés) de los Estados Unidos, que se estaban retirando un gran numero de cantidad de estas pruebas caseras, ya que algunas de ellas eran falsas y no contar con la autorización del máximo organismo.
En específico la FDA en su comunicado se refirió a las pruebas ACON Flowflex COVID-19 del laboratorio ACON Biotech. Ante este informe, la compañía ACON Laboratories Inc., dijo que identificaron la ” venta ilegal de una copia mal hecha de un producto que no está aprobado por la FDA y con el que todavía trabaja en sus laboratorios”, informó ViveUSA.
Por su parte, la FDA recalcó que la este prueba ‘falsa’ no ha sido aprobado ni autorizada para distribuirse en los Estados Unidos, y que hay una gran preocupación por los resultados inexactos que podría arrojar la misma, debido a ser un producto de “mala calidad”, dando falsos positivos o falsos negativos.
De acuerdo con el comunicado de las autoridades esta prueba ha sido “adulterado y mal etiquetado con el nombre comercial Prueba rápida de antígeno Flowflex SARS-CoV-2 (autoevaluación)”, las cuales han sido repartidas en varios estados del país.
“La prueba rápida del antígeno SARS-CoV-2 (autoevaluación) no se puede importar, distribuir ni utilizar legalmente en el mercado de Estados Unidos, ya que no ha sido aprobada o autorizada por la FDA”, afirmaron las autoridades de salud. De igual manera, añadieron en el informe que las copias falsas están empaquetadas en cajas azules con el nombre en inglés “Flowflex SARS-CoV-” Antigen Rapid Test (Self-Testing), mientras que las pruebas originales y autorizadas vienen en cajas blancas con el nombre en inglés “Flowflex Covid-19 Antigen Home Test”.
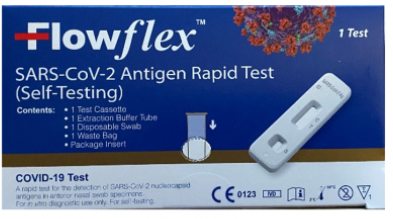
FDAEtiqueta del frente de la caja

FDAEtiqueta de la parte posterior de la caja
Por su parte la prueba casera de antígeno Flowflex COVID-19 de ACON Laboratories de caja blanca, autorizada por la FDA el 4 de octubre de 2021, no es objeto de este aviso y puede continuar usándose, aseguró ABC4.
¿Qué pasa con los pacientes que fueron testados con las pruebas falsas? De acuerdo con la FDA, recomiendan que las personas que recibieron este test falso en las ultimas dos semanas, que deben de asistir a su proveedor de atención médica y volver a recibir una evaluación con una de las pruebas autorizada por la FDA.
Si ha tenido problemas con una prueba de SARS-CoV-2, la FDA recomienda informar el problema a través del Formulario de informe voluntario de MedWatch. Se pueden enviar más preguntas por correo electrónico a la División de Industria y Educación del Consumidor (DICE) a DICE@FDA.HHS.GOV o llamando al 800-638-2041 o al 301-796-7100.
Cabe anotar que estas pruebas, las de caja azul, SÍ están reguladas legalmente en Europa, bajo el mismo nombre, pero no pueden “importarse, distribuirse o usarse legalmente” en los EE. UU., según el anuncio.
En el comunicado de la FDA se lee:
La Administración de Drogas y Alimentos de los EE. UU. (FDA) advierte a las personas que no usen ciertas pruebas ACON COVID-19, un producto de ACON Biotech (Hangzhou) Co., Ltd. Las personas no deben usar la prueba ACON Biotech llamada “Flowflex SARS-CoV- Prueba rápida de 2 antígenos (autoevaluación)” que se empaqueta en una caja azul oscuro (consulte las imágenes a continuación). Esta prueba no ha sido autorizada, autorizada o aprobada por la FDA para su distribución o uso en los Estados Unidos. La FDA está preocupada por el riesgo de resultados falsos al usar esta prueba no autorizada.
La FDA no ha recibido informes de lesiones, consecuencias adversas para la salud o muertes asociadas con el uso no autorizado de la prueba rápida de antígeno Flowflex SARS-CoV-2 de ACON Biotech (autoevaluación).
Recomendaciones:
Si tiene una prueba ACON Flowflex COVID-19, compare el empaque con la imagen de arriba. No utilice la prueba rápida de antígeno Flowflex SARS-CoV-2 de ACON Biotech (autoevaluación) en el empaque azul oscuro, como se muestra arriba.
Usuarios de la prueba y cuidadores: Hable con su proveedor de atención médica si cree que se le hizo la prueba con la prueba rápida de antígeno Flowflex SARS-CoV-2 de ACON Biotech (autoprueba) y tiene inquietudes sobre los resultados de la prueba.
Proveedores de atención médica y organizadores de programas de pruebas: si se realizó una prueba de antígeno hace menos de dos semanas con la prueba rápida de antígenos SARS-CoV-2 Flowflex de ACON Biotech (autoevaluación), considere volver a realizar la prueba a sus pacientes con una prueba de detección de antígenos SARS-CoV-2 autorizada por la FDA. 2 pruebas de diagnóstico si sospecha un resultado inexacto. Si la prueba se realizó hace más de dos semanas y no hay motivo para sospechar una infección actual por SARS-CoV-2, no es necesario volver a realizar la prueba.
Informe cualquier problema que experimente con la prueba rápida de antígeno Flowflex SARS-CoV-2 (autoevaluación) a la FDA, incluidos los presuntos resultados falsos. Consulte Cómo informar problemas con su prueba.
Descripción de la prueba:
La prueba rápida de antígeno Flowflex SARS-CoV-2 de ACON Biotech no autorizada (autoevaluación) utiliza una muestra de hisopo nasal para detectar proteínas, llamadas antígenos, del SARS-CoV-2, el virus que causa el COVID-19. La prueba no autorizada tiene un recuadro azul oscuro con letras y símbolos blancos en la esquina inferior derecha del recuadro, incluidas las letras “CE” y el nombre ACON Biotech (Hangzhou) Co., Ltd. identificado en la etiqueta exterior del recuadro.
La prueba casera de antígeno Flowflex COVID-19 de ACON Laboratories, autorizada por la FDA el 4 de octubre de 2021, no es objeto de este comunicado de seguridad y se puede seguir utilizando.
LEER MÁS: Buscan a un asesino serial de indigentes en Washington y Nueva York [VIDEO]

